
Stephan Wilkens, PhD
CURRENT APPOINTMENTS
LANGUAGES
研究项目和附属机构
RESEARCH INTERESTS
EDUCATION
RESEARCH ABSTRACT
 Our main focus is on the structure and mechanism of the eukaryotic proton pumping vacuolar ATPase (V-ATPase; V1Vo-ATPase). V-ATPase is a large, 多亚基膜蛋白复合物存在于所有真核细胞的膜系统中, 它在哪里起酸化胞内细胞器的作用, including endosomes, lysosomes, 高尔基体和突触囊泡. 这些腔室内的酸性pH值对包括内吞作用在内的基本细胞功能至关重要, protein degradation, protein trafficking, 神经递质负荷. 当在质膜上发现“专业”分泌酸的细胞,如骨破骨细胞和肾插层细胞, v - atp酶将质子泵到细胞外, 骨重塑和尿液酸化所必需的过程. 因为它参与了许多基本的细胞功能, v - atp酶功能失常会导致包括骨质疏松症在内的广泛的人类疾病, neurodegeneration, diabetes, cancer, and AIDS.
Our main focus is on the structure and mechanism of the eukaryotic proton pumping vacuolar ATPase (V-ATPase; V1Vo-ATPase). V-ATPase is a large, 多亚基膜蛋白复合物存在于所有真核细胞的膜系统中, 它在哪里起酸化胞内细胞器的作用, including endosomes, lysosomes, 高尔基体和突触囊泡. 这些腔室内的酸性pH值对包括内吞作用在内的基本细胞功能至关重要, protein degradation, protein trafficking, 神经递质负荷. 当在质膜上发现“专业”分泌酸的细胞,如骨破骨细胞和肾插层细胞, v - atp酶将质子泵到细胞外, 骨重塑和尿液酸化所必需的过程. 因为它参与了许多基本的细胞功能, v - atp酶功能失常会导致包括骨质疏松症在内的广泛的人类疾病, neurodegeneration, diabetes, cancer, and AIDS.
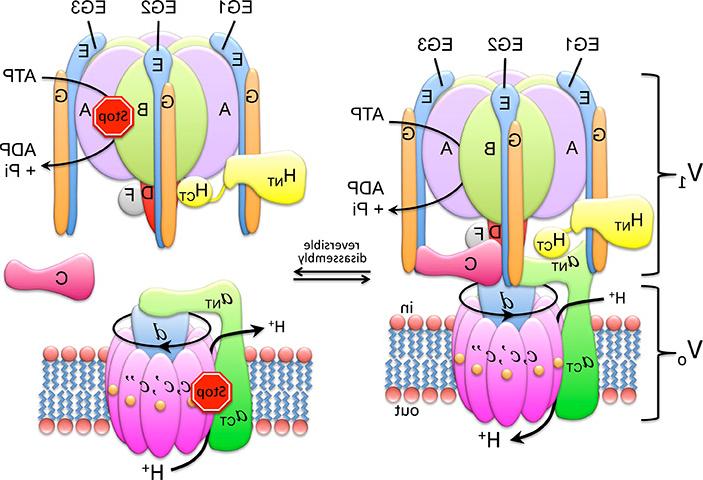
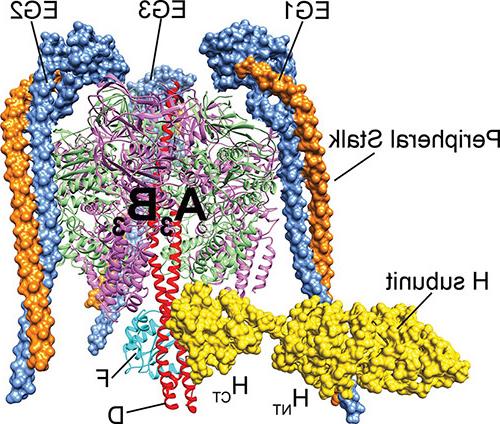 v - atp酶由两个旋转马达亚复合物组成, 一种膜外ATP水解v1 -ATP酶, 和一个嵌入膜的Vo质子涡轮. V1上的ATP水解与质子通过Vo的“中心柄”耦合,该“中心柄”以100 1/s的速度旋转,从细胞质溶胶中拾取质子,并将其运送到细胞器腔或细胞外. 作为细胞能量的主要消耗者, v - atp酶的功能受到一种称为“可逆分解”的机制的严格调节。. 当不需要酶的质子泵送时, V1与膜结合的Vo分离, 这两个亚复合物的活性被“沉默”,因此V1不再能够水解MgATP, Vo变得不被质子渗透. 可逆分解是真核生物v - atp酶所特有的,这一过程提供了一种调节引起v - atp酶的疾病活性以达到治疗目的的方法.
v - atp酶由两个旋转马达亚复合物组成, 一种膜外ATP水解v1 -ATP酶, 和一个嵌入膜的Vo质子涡轮. V1上的ATP水解与质子通过Vo的“中心柄”耦合,该“中心柄”以100 1/s的速度旋转,从细胞质溶胶中拾取质子,并将其运送到细胞器腔或细胞外. 作为细胞能量的主要消耗者, v - atp酶的功能受到一种称为“可逆分解”的机制的严格调节。. 当不需要酶的质子泵送时, V1与膜结合的Vo分离, 这两个亚复合物的活性被“沉默”,因此V1不再能够水解MgATP, Vo变得不被质子渗透. 可逆分解是真核生物v - atp酶所特有的,这一过程提供了一种调节引起v - atp酶的疾病活性以达到治疗目的的方法.
 我们的工作与v - atp酶从模式生物酿酒酵母(面包酵母)以及人类. 我们使用生物化学的工具,分子 & cell biology, 生物物理学和结构生物学(包括核磁共振波谱), x射线晶体学和低温电子显微镜(cryoEM),以获得结构和机械信息. 我们的长期目标是阐明V-ATPase独特的调节模式的机制,并在疾病状态下找到治疗靶向酶的方法.
我们的工作与v - atp酶从模式生物酿酒酵母(面包酵母)以及人类. 我们使用生物化学的工具,分子 & cell biology, 生物物理学和结构生物学(包括核磁共振波谱), x射线晶体学和低温电子显微镜(cryoEM),以获得结构和机械信息. 我们的长期目标是阐明V-ATPase独特的调节模式的机制,并在疾病状态下找到治疗靶向酶的方法.
Recent Publications
Sharma, S., Oot, R.A., Khan, Md M. and Wilkens, S. (2019) Vo质子通道和突变体V1-ATPase的液泡H+-ATPase功能重构为可逆分解调控机制提供了新的思路. J. Biol. Chem., in press.
Sharma, S., Oot, R.A. and Wilkens, S. (2018) MgATP水解破坏了H亚基与酵母v1 - atp酶之间的相互作用, 强调了H在v - atp酶可逆分解调控中的作用. J. Biol. Chem. 293, 10718-10730.
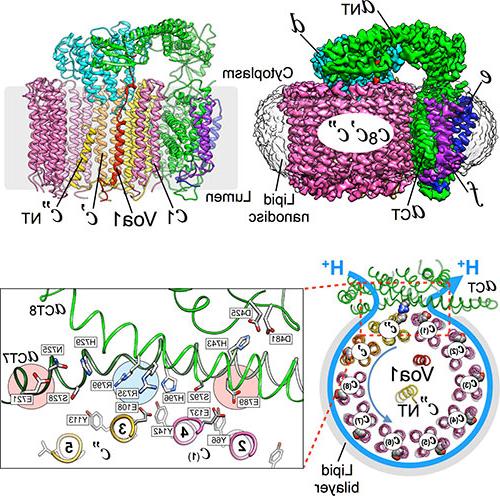
Roh, S.-H., Stam, N.J., Hryc, C., Couoh-Crdel, S., Pintillie, G, Chiu, W. and Wilkens, S. (2018) The 3.5-Å纳米圆盘重组酵母液泡atp酶Vo质子通道的低温结构. Mol. Cell 69, 993-1004.
Oot, R.A., Couoh-Cardel, S., Sharma, S., Stam, N.J. and Wilkens, S. (2017)《推荐最近最火的赌博软件》. Protein Science 26, 896-909.
Sharma, S. and Wilkens, S. (2017)脂质纳米圆盘重组酵母液泡H+- atp酶的生物层干涉测定. Protein Science 26, 1070-1079.
Stam, N.J. and Wilkens, S. (2017)纳米圆盘重组液泡atp酶质子通道的结构:转子和定子相互作用的定义及其对可逆解离酶调节的影响. J. Biol. Chem. 292, 1749-61.
Oot, R. A., Kane, P.M., Berry, E.A. and Wilkens, S. (2016)酵母v1 - atp酶在自抑制状态下的晶体结构. EMBO J. 35,1694-706.
Couoh-Cardel, S., Hsueh, Y.-C., Wilkens, S. and Movileanu, L. (2016)酵母v - atp酶蛋白脂环作为大导跨膜蛋白孔. Sci. Rep. 6, 24774.
